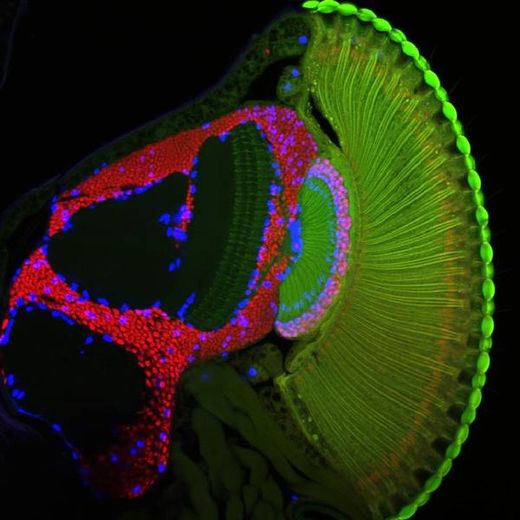
Es ist somit ganz essenziell, dass sich die richtigen Nervenzellen untereinander verbinden. Doch woher weiß das Axon, wann es aufhören sollte zu wachsen, um sich mit den umgebenden Zellen zu verknüpfen? Dieser Frage gingen Wissenschaftler des Max-Planck-Instituts für Neurobiologie mit Kollegen aus Kyoto auf den Grund. Sie untersuchten das visuelle System der Fruchtfliege und schauten sich ganz genau die Funktion der Gene an, die an der Entwicklung dieses Systems beteiligt sind.
Wie die Neurobiologen jetzt in der Fachzeitschrift Nature Neuroscience berichten, kann sich das visuelle System der Fruchtfliege nur dann richtig entwickeln, wenn zwei Gene zusammenarbeiten - die Gene, die für die Produktion der Proteine "Golden Goal" und "Flamingo" zuständig sind. Diese beiden Proteine befinden sich an der Spitze eines wachsenden Axons. Von hier sammeln sie Informationen über ihre Umgebung wahrscheinlich direkt aus dem umgebenden Gewebe. Das Verhalten dieser Proteine ermöglicht es den Nervenzellen, ihren Weg zu finden und ihr Ziel zu erkennen. Wie die Studie zeigte kommt es zum Chaos, wenn nur eines der beiden Gene aktiv, oder wenn ihr Zusammenspiel nicht richtig aufeinander abgestimmt ist: Die Axone stellen irgendwo unterwegs ihr Wachstum ein und können ihr Zielgebiet nicht erreichen.
"Wir gehen davon aus, dass ähnliche Mechanismen auch bei der Entwicklung von anderen Organismen - bis hin zum Menschen - eine Rolle spielen", erklärt Takashi Suzuki, der Leiter der Studie.
"Wir sind jetzt auf einem guten Weg zu verstehen, wie wir diese Zellen manipulieren können, damit sie auch sicher bis in ihr Zielgebiet wachsen."Dieses Wissen ist eine wichtige Grundlage für spätere Therapien bei Entwicklungsstörungen, die auf einem irregeleiteten Wachstum von Nervenzellen basieren. Auch als Orientierungshilfe für erneut auswachsende Nervenzellen nach einer Verletzung kann dieses Wissen bedeutend sein. (Max-Planck-Institut für Neurobiologie)
Originalveröffentlichung:
Hakeda-Suzuki S, Berger-Mueller S, Tomasi T, Usui T, Horiuchi S, Uemura T, Suzuki T. "Golden Goal Collaborates with Flamingo in Conferring Synaptic-Layer Specificity in the Visual System" Nature Neuroscience, 13. Februar 2011



Kommentare von Lesern
für unseren Newsletter an